Séquence n°2 - Etude des changements d'états physiques de l'eau sur Terre
I) Quels sont les changements d'état de l'eau possibles sur Terre ?
Activité n°4 :
Compétences travaillées :
- Utiliser un vocabulaire précis et adapté (D1)
- S'informer à partir d'un document, le conte (D1)
- Communiquer à l'oral, lecture (D1)
Activité n°4 :
Compétences travaillées :
- Utiliser un vocabulaire précis et adapté (D1)
- S'informer à partir d'un document, le conte (D1)
- Communiquer à l'oral, lecture (D1)
Bilan de l'activité n°4:
Le passage d'un état physique à un autre est appelé changement d'état physique.
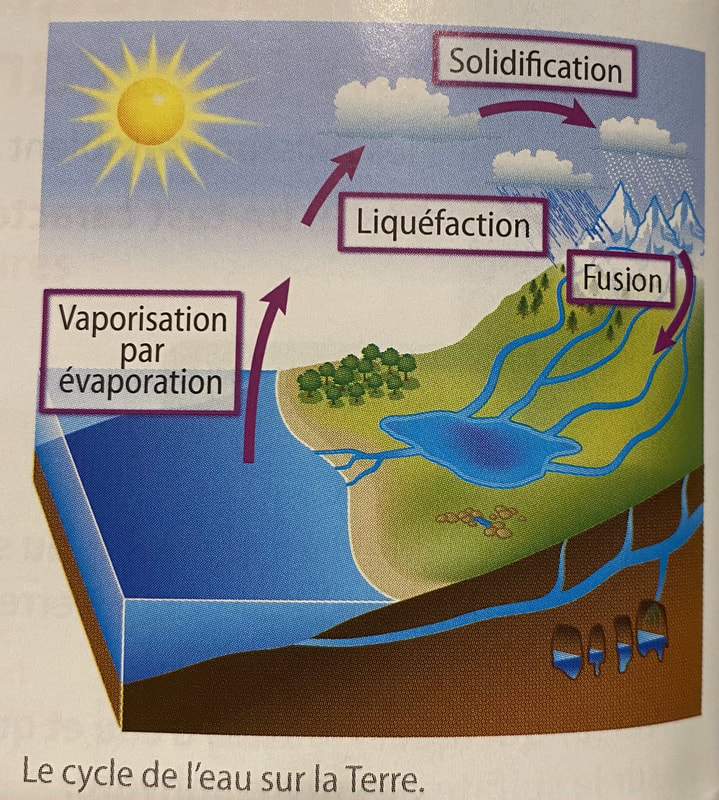
Dans la nature, après plusieurs changements d'états physiques (=transformations), l'eau revient à son état d'origine. On dit qu'elle parcourt un cycle dont le Soleil est le moteur. Les quatre changements d'état concernés sont: la fusion (S-> L), la solidification (L->S), la vaporisation (L->G) et la liquéfaction (G->L)
Le passage d'un état physique à un autre est appelé changement d'état physique.
Dans la nature, après plusieurs changements d'états physiques (=transformations), l'eau revient à son état d'origine. On dit qu'elle parcourt un cycle dont le Soleil est le moteur. Les quatre changements d'état concernés sont: la fusion (S-> L), la solidification (L->S), la vaporisation (L->G) et la liquéfaction (G->L)
Exercice associé à l'activité n°4 :
|
|
| ||||||
Ce qu'il faut retenir de l'exercice associé à l'activité n°4:
L'eau circule perpétuellement d'un réservoir à l'autre. Chaque réservoir gagne autant d'eau qu'il en perd. Par conséquence, la quantité d'eau présente dans chaque réservoir terrestre est constante, d'où l'appellation "cycle de l'eau".
L'eau circule perpétuellement d'un réservoir à l'autre. Chaque réservoir gagne autant d'eau qu'il en perd. Par conséquence, la quantité d'eau présente dans chaque réservoir terrestre est constante, d'où l'appellation "cycle de l'eau".
II) Etude de divers paramètres lors d'un changement d'état
a) Le volume et la masse varient-ils lors de la solidification de l'eau?
Activité n°5 Partie n°1 :
Compétences travaillées :
- Mettre en oeuvre une démarche scientifique (D4)
- Présenter une démarche scientifique à l'écrit (D1)
Activité n°5 Partie n°2 :
Compétences travaillées :
- Décrire, interpréter des résultats et tirer une conclusion (D4)
- Expliquer une expérience à l'oral (D1)
a) Le volume et la masse varient-ils lors de la solidification de l'eau?
Activité n°5 Partie n°1 :
Compétences travaillées :
- Mettre en oeuvre une démarche scientifique (D4)
- Présenter une démarche scientifique à l'écrit (D1)
Activité n°5 Partie n°2 :
Compétences travaillées :
- Décrire, interpréter des résultats et tirer une conclusion (D4)
- Expliquer une expérience à l'oral (D1)
Bilan de l'activité n°5:
Au cours de la solidification de l'eau, on observe que:
- La masse d'eau liquide est identique à la masse de glace. La masse se conserve car le nombre de molécules d'eau ne change pas. La masse se mesure avec une balance électronique.
- Le volume de l'eau liquide est différent de celui de la glace. Le volume varie car la distance entre les molécules varie. Le volume peut se mesurer avec divers instruments (fiche verrerie à connaitre).
C'est le cas pour n'importe quel changement d'état.
Au cours de la solidification de l'eau, on observe que:
- La masse d'eau liquide est identique à la masse de glace. La masse se conserve car le nombre de molécules d'eau ne change pas. La masse se mesure avec une balance électronique.
- Le volume de l'eau liquide est différent de celui de la glace. Le volume varie car la distance entre les molécules varie. Le volume peut se mesurer avec divers instruments (fiche verrerie à connaitre).
C'est le cas pour n'importe quel changement d'état.
Fiche présentant la verrerie du chimiste (noms et dessins à connaitre):
| verrerie_chimie.pdf |
b) Comment la température de l'eau évolue-t-elle lors de l'ébullition ?
Activité n°6:
Compétences travaillées:
- Mettre en œuvre un protocole expérimental de mesure (D4)
- Réaliser des mesures : la température (D2)
- Communiquer à l’aide d’un graphique (D1)
Compétences travaillées:
- Mettre en œuvre un protocole expérimental de mesure (D4)
- Réaliser des mesures : la température (D2)
- Communiquer à l’aide d’un graphique (D1)
Bilan de l'activité n°6 :
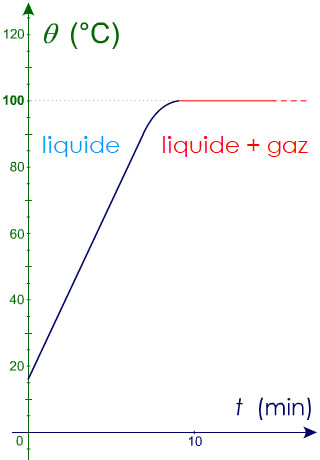
Lorsqu'on chauffe (ou refroidit) un corps pur, on lui apporte (ou retire) de l'énergie thermique. Ce transfert d'énergie se traduit par une augmentation (ou diminution) de température jusqu'à un palier horizontal de température: c'est la température de changement d'état.
Les changements d'états des corps purs s'effectuent à température constante.
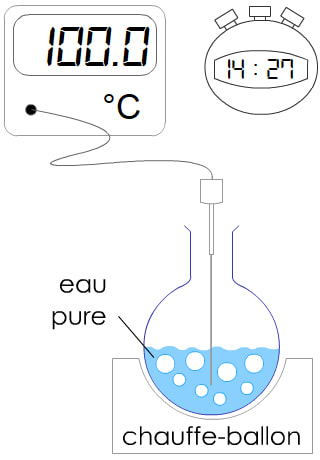
L'ébullition de l'eau pure (= ne contenant que des molécules d'eau, pas de sels ni minéraux) a lieu à 100°C.
Lorsqu'on chauffe (ou refroidit) un corps pur, on lui apporte (ou retire) de l'énergie thermique. Ce transfert d'énergie se traduit par une augmentation (ou diminution) de température jusqu'à un palier horizontal de température: c'est la température de changement d'état.
Les changements d'états des corps purs s'effectuent à température constante.
L'ébullition de l'eau pure (= ne contenant que des molécules d'eau, pas de sels ni minéraux) a lieu à 100°C.
Rappel: CORPS PUR/MÉLANGE
Un corps pur est une substance composée d'un seul type de molécules tandis qu'un mélange est composé de plusieurs types de molécules.
Un corps pur est une substance composée d'un seul type de molécules tandis qu'un mélange est composé de plusieurs types de molécules.
Activité de reprise Nov 2023:
| act_reprise_.pdf |
Ce qu'il faut retenir de l'activité de reprise :
Lorsqu'on chauffe (ou refroidit) un corps pur, on lui apporte (ou retire) de l'énergie thermique. Ce transfert d'énergie se traduit par une augmentation (ou diminution) de température jusqu'à un palier horizontal de température: c'est la température de changement d'état.
Les changements d'états des corps purs s'effectuent à température constante.
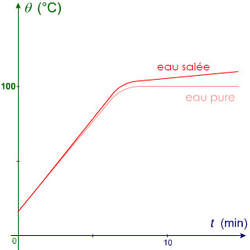
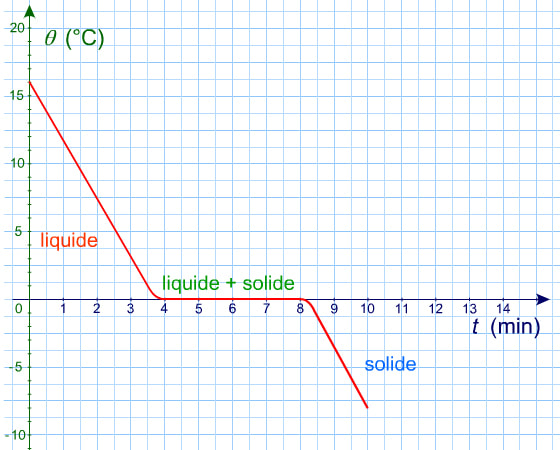
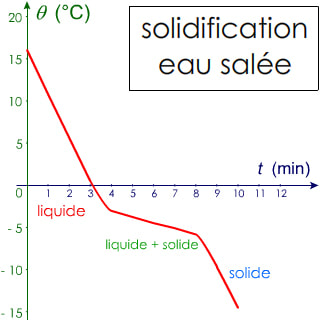
La solidification (ou la fusion) de l'eau pure (= ne contenant que des molécules d'eau, pas de sels ni minéraux) se déroule à 0°C. On voit donc un palier de température horizontal à 0°C sur le graphique. Ce n'est pas le cas pour l'eau salée puisque c'est un mélange.
Lorsqu'on chauffe (ou refroidit) un corps pur, on lui apporte (ou retire) de l'énergie thermique. Ce transfert d'énergie se traduit par une augmentation (ou diminution) de température jusqu'à un palier horizontal de température: c'est la température de changement d'état.
Les changements d'états des corps purs s'effectuent à température constante.
La solidification (ou la fusion) de l'eau pure (= ne contenant que des molécules d'eau, pas de sels ni minéraux) se déroule à 0°C. On voit donc un palier de température horizontal à 0°C sur le graphique. Ce n'est pas le cas pour l'eau salée puisque c'est un mélange.
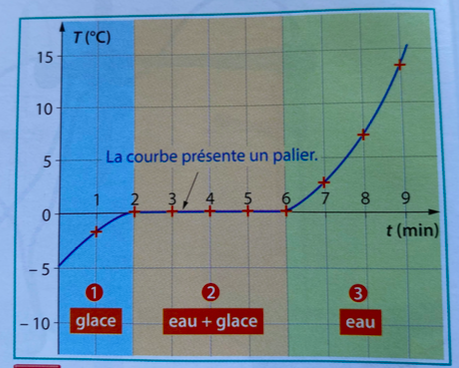
Autre exemple de courbe de température: Celle de la fusion de la glace
Pour en savoir plus, clique sur le lien ci-dessous
c) L'eau pure bout-elle toujours à la température de 100°C ?
Activité n°7:
Compétences travaillées:
- S'informer à partir d'une vidéo (D1)
- Expliquer un phénomène à l'écrit (D1)
Activité n°7:
Compétences travaillées:
- S'informer à partir d'une vidéo (D1)
- Expliquer un phénomène à l'écrit (D1)
|
Bilan de l'activité n°7 :
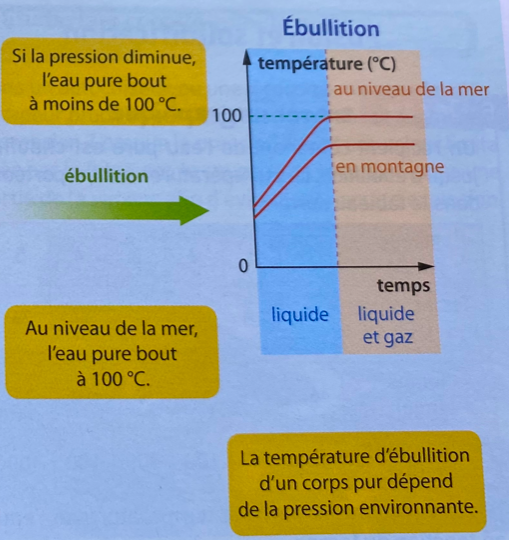
La température de changement d'état de l'eau pure dépend de la pression de l'environnement: si la pression diminue (en montagne par exemple), la température d'ébullition de l'eau pure diminue, le palier de température est donc situé plus bas sur le graphique donnant T en fonction de t. |
Tu souhaites en savoir plus à propos des effets de la pression sur la température de changement d'état de l'eau? Lis le document ci-dessous.
Contrat de révision S2 :