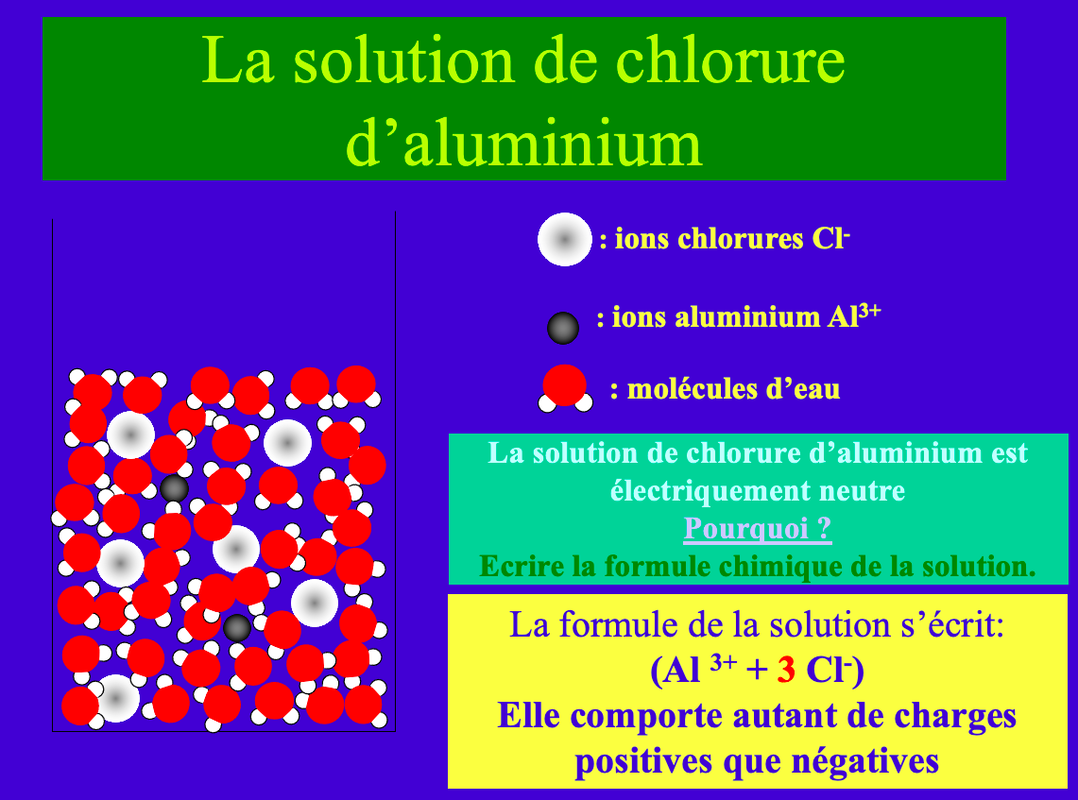
Séquence n°3 - Prévention et dangers liés aux solutions ioniques
Besoin d'un rafraîchissement concernant les ions ? Clique sur la case orange ci-dessous:
I) Lorsqu'on manipule une solution ionique, pensons à étiqueter le flacon!
Préparation de l'activité n°7: Fiche méthode concernant les tests caractéristiques de 4 ions
| tests_caracteristiques_ions.pdf |
Activité n°7 - "Étiquetons tous les flacons pour notre sécurité"
Activité en classe, en groupe
Compétences travaillées :
- Mettre en oeuvre un protocole expérimental
- Travailler en groupe de façon efficace
Manipulation de diverses solutions de façon à répondre à un problème scientifique. Les élèves sont amenés à réaliser des tests mettant en évidence la présence des ions classiques
Activité en classe, en groupe
Compétences travaillées :
- Mettre en oeuvre un protocole expérimental
- Travailler en groupe de façon efficace
Manipulation de diverses solutions de façon à répondre à un problème scientifique. Les élèves sont amenés à réaliser des tests mettant en évidence la présence des ions classiques
Bilan de l'activité n°7:
--> Le Nitrate d'Argent est le réactif caractéristique des ions Chlorure de formule Cl-
--> L'Hydroxyde de Sodium (= Soude) est le réactif caractéristique des ions métalliques: Cuivre(II) de formule Cu2+, Fer(II) de formule Fe2+ et Fer(III) de formule Fe3+
L'utilisation de quelques gouttes de réactif entraîne la formation d'un précipité coloré, ce qui permet de reconnaître l'ion présent dans la solution ionique testée.
Pour notre sécurité, il faut toujours penser à étiqueter tout flacon contenant ces ions métalliques: on y écrit par exemple le nom de la solution ionique ainsi que les formules du cation et de l'anion la composant.
--> Le Nitrate d'Argent est le réactif caractéristique des ions Chlorure de formule Cl-
--> L'Hydroxyde de Sodium (= Soude) est le réactif caractéristique des ions métalliques: Cuivre(II) de formule Cu2+, Fer(II) de formule Fe2+ et Fer(III) de formule Fe3+
L'utilisation de quelques gouttes de réactif entraîne la formation d'un précipité coloré, ce qui permet de reconnaître l'ion présent dans la solution ionique testée.
Pour notre sécurité, il faut toujours penser à étiqueter tout flacon contenant ces ions métalliques: on y écrit par exemple le nom de la solution ionique ainsi que les formules du cation et de l'anion la composant.
II) Une solution ionique est dangereuse car elle est conductrice d'électricité !
Préparation de l'activité n°8: Fiche méthode "Comment écrire une équation de réaction incluant des molécules/atomes ou ions?"
| fiche_methode_equation_3eme.pdf |
Besoin d'un peu d'entrainement sur les équations de réaction à ajuster??? Clique sur les deux vignettes ci-dessous pour découvrir deux exercices supplémentaires facultatifs:
Activité n°8 - "Enquête sur un accident domestique tragique"
Bilan de l'activité n°8:
Une solution ionique est conductrice d'électricité, ce qui la rend dangereuse: les ions qui s'y trouvent, placés dans la cuve à électrolyse, peuvent transporter le courant électrique et prennent part à une transformation chimique.
La méthode d'écriture d'une équation de transformation chimique est à maitriser.
Une solution ionique est conductrice d'électricité, ce qui la rend dangereuse: les ions qui s'y trouvent, placés dans la cuve à électrolyse, peuvent transporter le courant électrique et prennent part à une transformation chimique.
La méthode d'écriture d'une équation de transformation chimique est à maitriser.
III) Certaines solutions ioniques dites acides et basiques peuvent être responsables d’accidents domestiques
Préparation de l'activité n°9: Ce que je dois savoir à propos des solutions acides, basiques et neutres.
Qu'appelle-t-on acide? Qu'appelle-t-on base?
Une solution aqueuse peut être acide, neutre ou basique. C’est le pH de la solution qui nous indique le caractère acide, neutre ou basique d’une solution. Le pH est une grandeur qu’on peut évaluer soit à l’aide de papier pH soit à l’aide d’un appareil appelé pH-mètre.
Une solution aqueuse peut être acide, neutre ou basique. C’est le pH de la solution qui nous indique le caractère acide, neutre ou basique d’une solution. Le pH est une grandeur qu’on peut évaluer soit à l’aide de papier pH soit à l’aide d’un appareil appelé pH-mètre.
Activité n°9 - "Menons l'enquête"
Activité en classe, en groupe
Compétences travaillées :
- Mettre en oeuvre un protocole expérimental
- Travailler en groupe de façon efficace
- Communiquer à l'aide d'un schéma
Manipulation de diverses solutions de façon à répondre à un problème scientifique. Les élèves sont amenés à réaliser des tests mettant en évidence le caractère acide/basique/neutre de 3 solutions de la vie courante: l'eau de javel, l'eau déminéralisée et le déboucheur.
Activité en classe, en groupe
Compétences travaillées :
- Mettre en oeuvre un protocole expérimental
- Travailler en groupe de façon efficace
- Communiquer à l'aide d'un schéma
Manipulation de diverses solutions de façon à répondre à un problème scientifique. Les élèves sont amenés à réaliser des tests mettant en évidence le caractère acide/basique/neutre de 3 solutions de la vie courante: l'eau de javel, l'eau déminéralisée et le déboucheur.
Bilan de l'activité n°9:
Les solutions acides et basiques sont dangereuses lorsqu'elles sont corrosives ( = qui rongent). De plus, le contact avec des acides dits "concentrés" et des bases dites "concentrées" peut provoquer de graves brûlures de la peau, des muqueuses et des yeux. Il faut alors se protéger en portant des gants, des lunettes et une blouse.
Les solutions acides et basiques sont dangereuses lorsqu'elles sont corrosives ( = qui rongent). De plus, le contact avec des acides dits "concentrés" et des bases dites "concentrées" peut provoquer de graves brûlures de la peau, des muqueuses et des yeux. Il faut alors se protéger en portant des gants, des lunettes et une blouse.
Exercice de réinvestissement à propos du pH, suite à l'activité n°9:
| exercice_n°1_-_ph.pdf |
Activité n°10: "Que se passe-t-il lorsqu'on mélange une solution acide avec une solution basique?
Activité en classe, en groupe
Compétences travaillées : S'informer à partir d'un graphique
Activité en classe, en groupe
Compétences travaillées : S'informer à partir d'un graphique
| 30_x_act_10_-_année_2018_2019.pdf |
Bilan de l'activité n°10:
Lorsqu'on verse une solution basique dans une solution acide, le pH augmente, passe par 7 et continue d'augmenter si on verse beaucoup de solution basique.
Lorsqu'on verse une solution acide dans une solution basique, le pH diminue, passe par 7 et continue de diminuer si on verse beaucoup de solution acide.
Lorsqu'on verse de l'eau dans une solution acide ou une solution basique, le pH se rapproche de 7, pH de l'eau.
Une transformation/réaction chimique a alors lieu.
Lorsqu'on verse une solution basique dans une solution acide, le pH augmente, passe par 7 et continue d'augmenter si on verse beaucoup de solution basique.
Lorsqu'on verse une solution acide dans une solution basique, le pH diminue, passe par 7 et continue de diminuer si on verse beaucoup de solution acide.
Lorsqu'on verse de l'eau dans une solution acide ou une solution basique, le pH se rapproche de 7, pH de l'eau.
Une transformation/réaction chimique a alors lieu.
Exercices de réinvestissement associés à l'activité n°10 :
Pour faire les exercices en lien avec l'activité n°11, nous allons nous aider de la fiche méthode ci-dessous: "Comment écrire une équation de réaction correctement?"
| fiche_methode_3eme.pdf |
| 30_série_dexos_associés_à_lact_10.pdf |
Ce qu'il faut retenir de ces exercices:
Toute transformation chimique peut être représentée par deux écritures symboliques: l'équation et le bilan de transformation chimique (voir fiche méthode)
- L’équation précise le sens de la transformation chimique. Attention, celle-ci doit toujours être ajustée pour être valable et respecte donc le principe de conservation de la matière et de la charge.
- Le bilan de la réaction s'écrit uniquement en utilisant les noms des espèces chimiques mises en jeu.
Seuls les réactifs et produits sont utilisés pour écrire une équation ou un bilan. Les espèces spectatrices sont dissimulées.
Toute transformation chimique peut être représentée par deux écritures symboliques: l'équation et le bilan de transformation chimique (voir fiche méthode)
- L’équation précise le sens de la transformation chimique. Attention, celle-ci doit toujours être ajustée pour être valable et respecte donc le principe de conservation de la matière et de la charge.
- Le bilan de la réaction s'écrit uniquement en utilisant les noms des espèces chimiques mises en jeu.
Seuls les réactifs et produits sont utilisés pour écrire une équation ou un bilan. Les espèces spectatrices sont dissimulées.
IV) Une solution ionique peut parfois être responsable d’explosions.
Activité n°11 : "Que se passe-t-il lorsqu'on mélange une solution acide avec un métal ?
Activité en classe, en groupe
Compétences travaillées :
Activité en classe, en groupe
Compétences travaillées :
Ce qu'il faut retenir de l'activité n°11 :
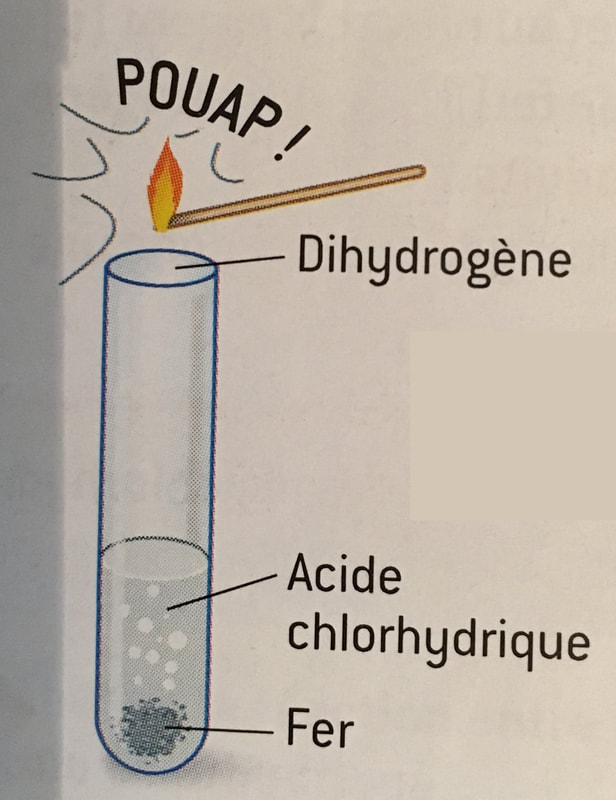
Lorsqu’on mélange de l’Acide Chlorhydrique et du Fer, il se produit une transformation chimique. Il se forme alors du Dihydrogène et des ions Fer(II)
- Le Dihydrogène peut être mis en évidence par le test de la flamme qui entraine une légère détonation
- Les ions Fer(II) peuvent être mis en évidence par le test à la Soude qui donne un précipité verdâtre.
Lorsqu’on mélange de l’Acide Chlorhydrique et du Fer, il se produit une transformation chimique. Il se forme alors du Dihydrogène et des ions Fer(II)
- Le Dihydrogène peut être mis en évidence par le test de la flamme qui entraine une légère détonation
- Les ions Fer(II) peuvent être mis en évidence par le test à la Soude qui donne un précipité verdâtre.
SI VOUS AVEZ BESOIN DE VOUS REENTRAINER SUR LES EQUATIONS DE REACTION, RDV DANS LA PARTIE PLAN DE COURS SEQUENCE 3 DES CLASSES DE 4eme
Exercice supplémentaire en lien avec l'activité n°11: "Des canettes plutôt étranges"
| exo_act_10_canette_en_lien_metal_acide.pdf |
POUR INFORMATION : Le chou rouge est un indicateur de pH très efficace!
Attention, dans cette activité, nous manipulons une solution basique dangereuse. Pour cela, je m'équipe de gants de lunettes et d'une blouse!
Présentation des solutions du quotidien testées:
De la gauche vers la droite: Produit vaisselle - vinaigre blanc - ammoniac - eau déminéralisée - déboucheur - lait- jus de citron - détartrant - café
De la gauche vers la droite: Produit vaisselle - vinaigre blanc - ammoniac - eau déminéralisée - déboucheur - lait- jus de citron - détartrant - café
Création de l'échelle de teinte, après ajout du chou rouge:
Le chou rouge change de couleur au contact des solutions testées et permet de ranger des solutions de la plus acide à la plus basique rien qu'en utilisant la couleur. Pratique! On dit qu'on crée une échelle de teinte.
Le chou rouge change de couleur au contact des solutions testées et permet de ranger des solutions de la plus acide à la plus basique rien qu'en utilisant la couleur. Pratique! On dit qu'on crée une échelle de teinte.
De la gauche vers la droite: Jus de citron - Détartrant - Vinaigre blanc - Café - Lait - eau déminéraliséeLiquide vaisselle - Ammoniac - Déboucheur
Résumé des résultats de l'expérience présentée :
DM numéro 2 sur les solutions acides et basiques: A VENIR
Contrat de révision en lien avec la séquence n°3 :